Что важно знать пациентам с заболеваниями сердца и сосудов
«Гипертония»
Термин «гипертония» или «давление», часто употребляемый пациентами, как правило, подразумевает постоянное или периодическое повышение артериального давления. Это состояние, при котором кровь, проходя по артериям всего тела, оказывает на них слишком большое давление, врачи называют «артериальная гипертензия» (АГ).
Относительно редко (5-10% случаев) АГ является вторичной, т.е. развивается вследствие заболеваний внутренних органов (почек, сердца, сосудов, щитовидной железы, надпочечников и др.).
Гораздо чаще АГ возникает вследствие совокупности факторов риска, набор которых отличается у разных людей. В этих случаях мы говорим о первичной артериальной гипертензии или гипертонической болезни.
Это самое распространенное хроническое неинфекционное заболевание в мире. При этом, каждый случай уникален: лечение, которое подошло одному пациенту, может не подойти другому.
Артериальное давление выше нормы может вызывать головные боли, ощущение сдавления или «напряжения в голове», головокружение и утомляемость, сердцебиение. Нередко пациенты не обращают на них внимания. Более того, стойкая АГ может долго никак себя не проявлять, и Вы можете не подозревать о ее наличии. Однако даже при отсутствии симптомов и жалоб врач на приеме может определить ее наличие путем измерения артериального давления в состоянии покоя с помощью тонометра.
Может оказаться, что повышения артериального давления имеют эпизодический характер в виде нормальной реакции на эмоциональные переживания, стрессовые ситуации. Сам осмотр врача может быть фактором стресса («синдром белого халата»). Однако, когда цифры артериального давления часто или стойко выше нормальных значений, в том числе в состоянии покоя, вероятнее всего речь идет о заболевании.
Пациенту бывает сложно поверить в высокие цифры артериального давления при измерении у врача либо самостоятельно, ведь «самочувствие абсолютно нормальное». К сожалению, без лечения и профилактики АГ со временем вызывает серьезные осложнения – инфаркты, инсульты, заболевания сосудов, сердечную и почечную недостаточность и другие.
Доказано, что нормализация артериального давления путем приема лекарств и коррекции образа жизни существенно снижает риск этих осложнений. Следовательно, если у Вас есть АГ – с ней можно и нужно бороться.
Для поддержания нормального профиля артериального давления во многих случаях потребуется длительный или постоянный прием лекарственных препаратов. Некоторые пациенты перестают принимать препараты по выходным или в отпуске, так как убеждены, что в спокойной обстановке АД снижается естественным путем. Окружающая обстановка может влиять на цифры АД у гипертоников как в сторону снижения, так и в сторону повышения, и это подчеркивает необходимость беспрерывного приема терапии.
Терапия может иметь побочные эффекты, вероятность которых пациент должен иметь ввиду и обязательно сообщать лечащему врачу об их появлении.
Существуют факторы риска, повышающие артериальное давление (рис. 1). Те, на которые Вы повлиять не можете – немодифицируемые. К ним относятся возраст и пол. В этом смысле чаще от гипертонии страдают мужчины, лица старше 40-45 лет, а также люди с отягощенной наследственностью по этому заболеванию (АГ у близких родственников).
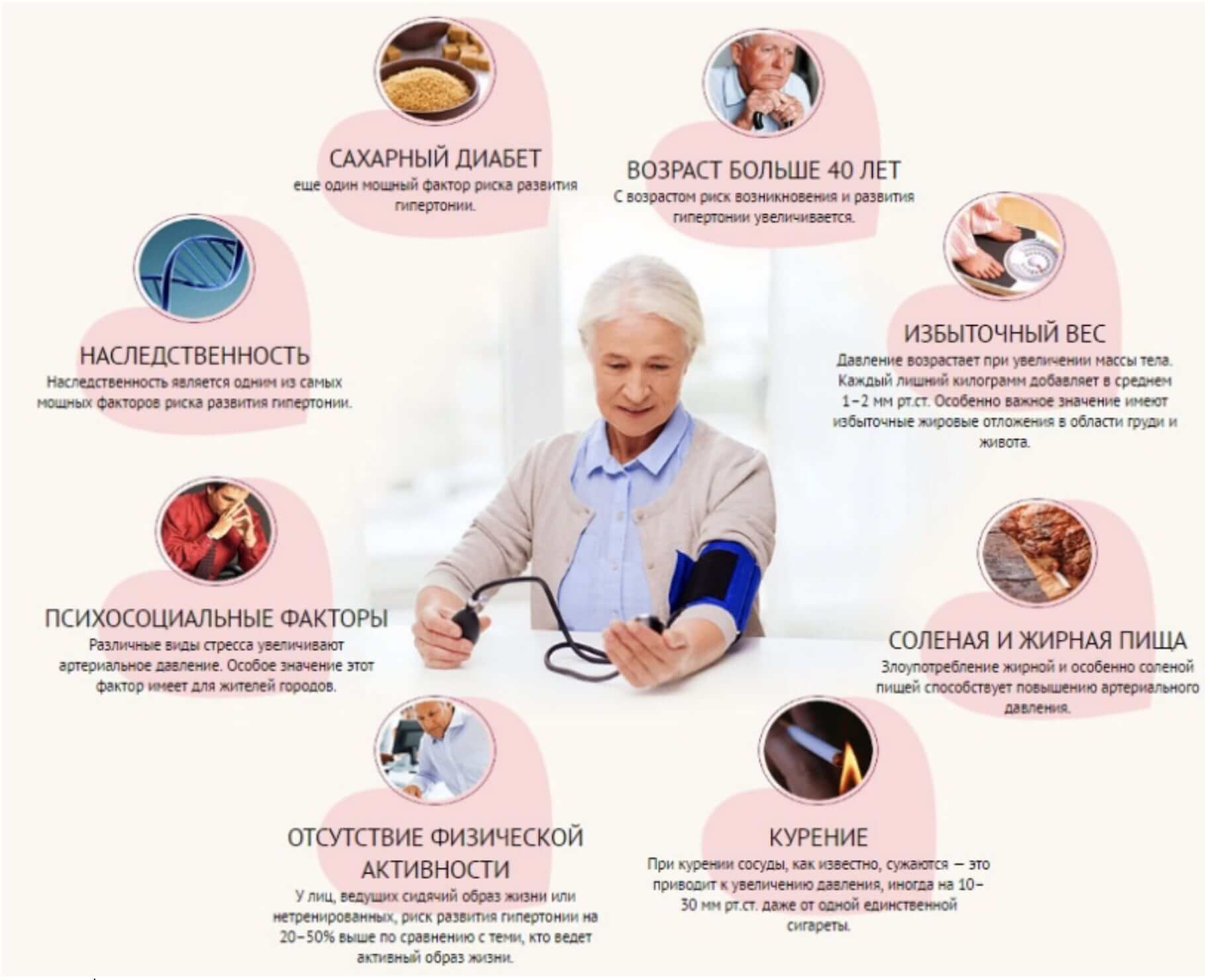
Рисунок 1. Факторы риска гипертонической болезни.
Гораздо больше факторов риска являются модифицируемыми. Это значит, что Вы можете их устранить, изменив образ жизни. К ним относят курение и употребление алкоголя, низкую физическую активность, ожирение, употребление в пищу животных жиров и большого количества соли.
Отказавшись от табака и алкоголя, увеличив продолжительность и количество прогулок, а также прибегнув к другим видам аэробной динамической активности (плавание, езда на велосипеде, бег трусцой и т.п.), оздоровив пищевые привычки и удерживая в норме свой вес, Вы можете привести артериальное давление к нормальным цифрам или, по крайней мере, существенно его снизить.
Существует множество схем лечения, которые включают и медикаментозную терапию, и оздоравливающие образ жизни мероприятия. Конечная цель лечебного процесса – улучшение качества и продолжительности жизни. Этому способствует выбор, иногда – после неоднократных корректировок, наиболее комфортной схемы лечения, основанной на индивидуальных особенностях и потребностях пациента.
Обсудите с врачом все аспекты лечения и профилактики применительно к вашей жизненной ситуации. Отнеситесь внимательно к рекомендациям врача – это лучшее, что Вы можете сделать для сохранения своего здоровья.
Ишемическая болезнь сердца
Стенокардия («грудная жаба»)
Стенокардия – внезапная боль в груди вследствие недостаточного поступления кислорода в сердечную мышцу (миокард). Просторечное, старое понятие «грудная жаба» описывает сочетание боли с ощущением сдавления и затруднением дыхания (рис. 2). Иногда боль распространяется и за пределы грудной клетки. Существует немало причин боли в грудной клетке, но в первую очередь мы думаем о стенокардии и связанном с ней риске инфаркта.

Рисунок 2. Больной с приступом стенокардии.
Кислородное голодание (ишемия) миокарда развивается при сужении артерий, приносящих кровь, обогащенную кислородом (коронарных артерий). Причиной сужения коронарных артерий в абсолютном большинстве случаев является атеросклероз (рис. 3). Если атеросклеротическая бляшка, которая может иметь разную форму и протяженность, сужает просвет сосуда на 70% и более, это приводит к ишемии миокарда, как правило, проявляющейся периодически возникающим характерным болевым синдромом.
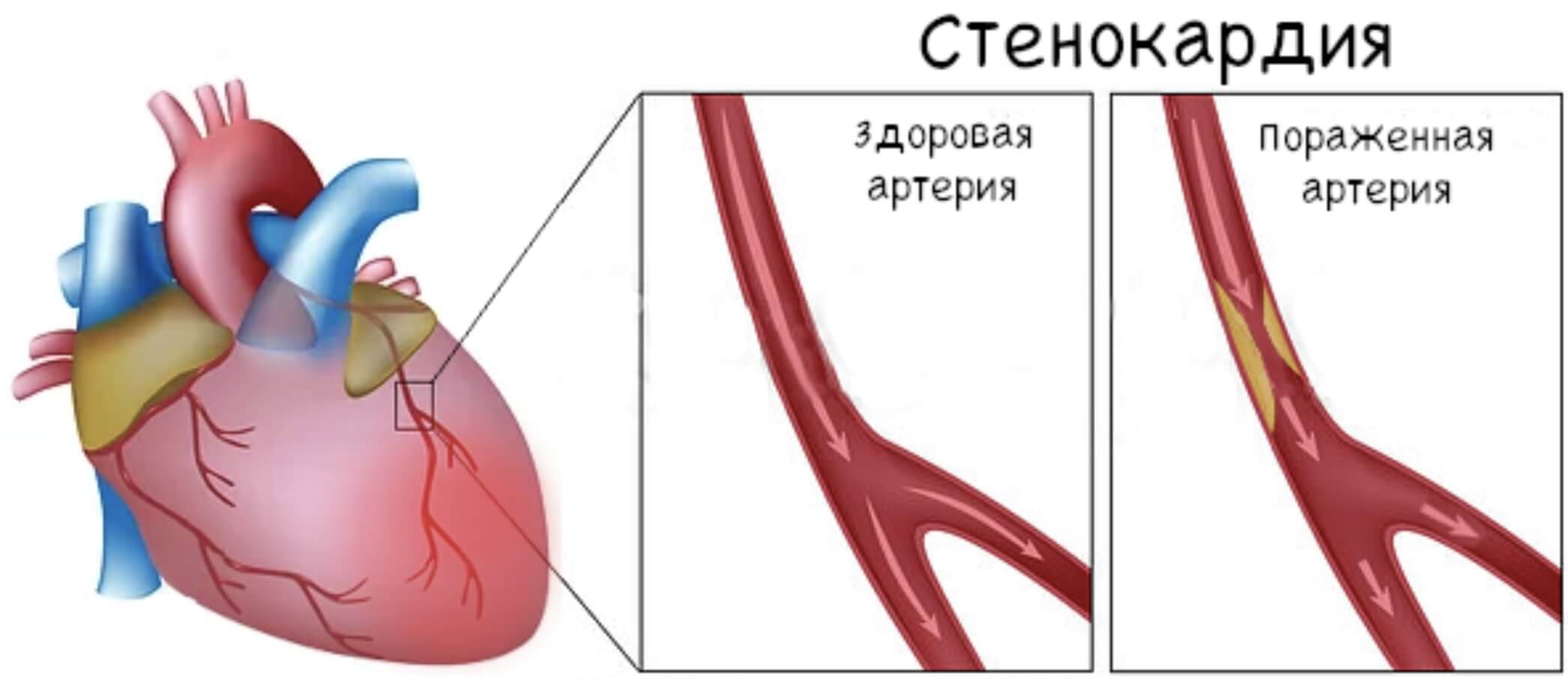
Рисунок 3. Атеросклероз коронарных артерий как причина ишемической болезни сердца.
Обычно боль возникает при увеличении нагрузки на сердце – во время физической активности и психоэмоционального напряжения (стенокардия напряжения), а иногда может наблюдаться в покое. Важно, как можно быстрее прекратить любую нагрузку, после чего боль должна пройти в течение нескольких минут. Если приступ стенокардии не проходит самостоятельно в течение 20 минут, стоит вызвать бригаду скорой медицинской помощи. Симптомы стенокардии игнорировать нельзя – без профилактики и лечения она приводит к инфаркту миокарда.
Приступ стенокардии можно снять быстродействующими лекарствами – обычно в виде спрея под язык. Эти препараты расширяют коронарные артерии и восстанавливают ток крови. Такое лекарство пациенты с установленным диагнозом должны всегда иметь при себе. Однако, бороться необходимо не с последствиями, а с причиной, то есть с сужением одной или нескольких артерий.
Иногда болевой синдром отсутствует, чаще у мужчин и больных сахарным диабетом. При этом пациент может испытывать эквивалент боли – одышку ± кашель при физической нагрузке или волнении. Безболевая ишемия миокарда нередко приводит к позднему обращения к врачу, порой, к сожалению, уже с острым инфарктом миокарда, что создает дополнительные риски для жизни и здоровья.
Профилактика и лечение стенокардии предполагает прежде всего изменение образа жизни: отказ от курения, диету с пониженным содержанием холестерина и регулярную физическую активность.
Прием лекарств, улучшающих ток крови и/или снижающих потребность сердца в кислороде, а также препаратов, защищающих клетки миокарда от ишемии (метаболические препараты) позволяет улучшить переносимость нагрузок.
Однако в данном случае важно попытаться не допустить осложнений в виде инфаркта миокарда. В этом помогут препараты, препятствующие дальнейшему росту атеросклеротических бляшек, формированию тромбов в сосудах сердца, способствующие нормализации артериального давления.
Коронароангиография. Врач-кардиолог может назначить коронароангиографию (КАГ) – рентгенологическое исследовании, при котором в отделении рентгенэндоваскулярной диагностики под местной анестезией с помощью тонкого катетера, проведенного через бедренную или лучевую артерии, в сосуды сердца вводится контраст на основе йода, проявляющий суженные участки коронарного сосудистого русла (рис. 4, 5, 6).
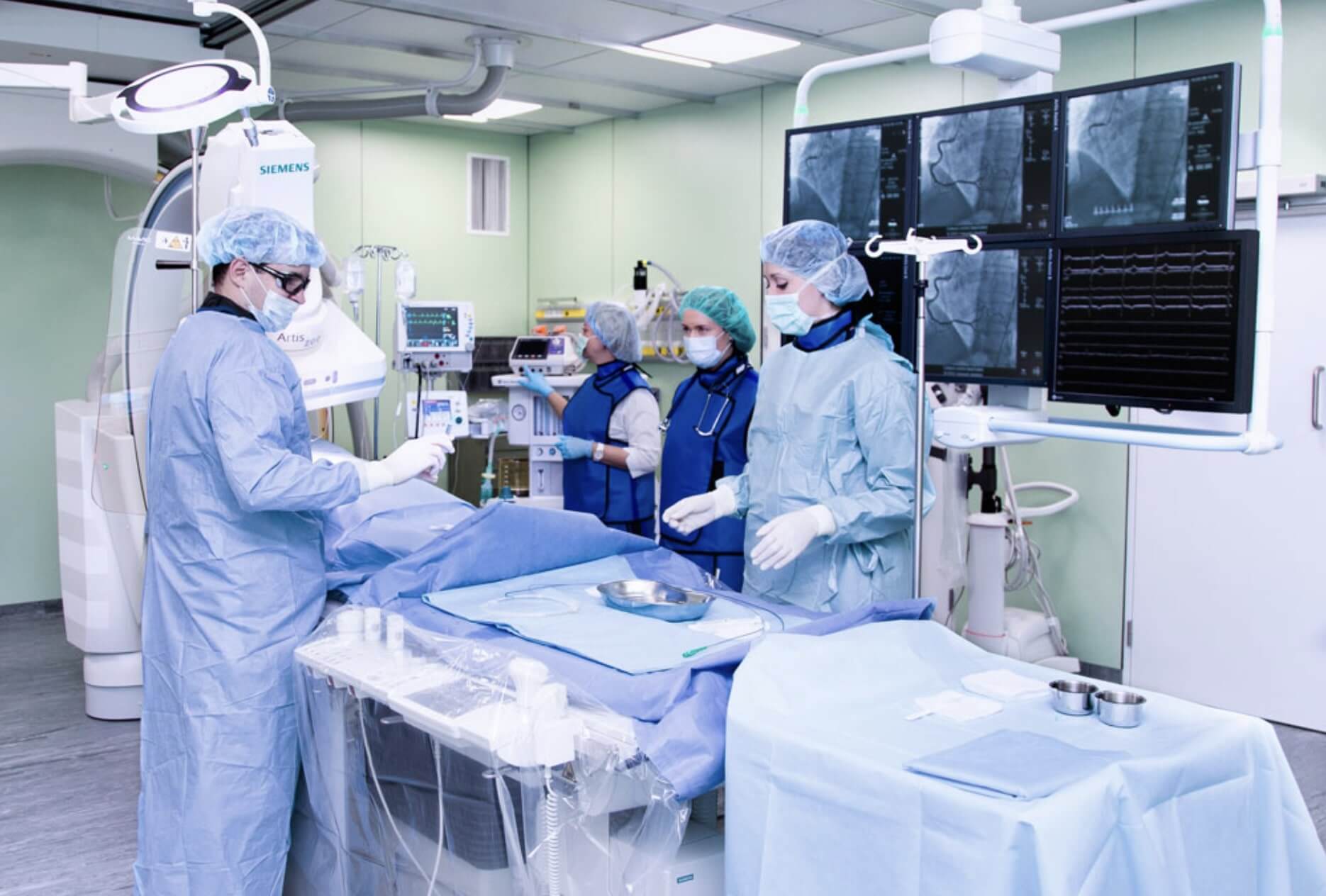
Рисунок 4. Процедура диагностической коронароангиографии в рентген-операционной.

Рисунок 5. Схема проведения катетера при коронароангиографии.

Рисунок 6. Коронарное русло при введении рентгенопозитивного контрастного вещества.
Пункция периферической артерии проводится под местным обезболиванием. Сама по себе процедура ввода контрастного вещества безболезненна – обычно больные лишь чувствуют тепло в этот момент.
Чрезкожное коронарное вмешательство (ангиопластика и стентирование) позволяет при необходимости устранить выявленные при коронароангиографии участки сужений. Если просвет сосуда слишком мал (стеноз артерии), его расширяют специальным устройством – баллоном, который находится на конце катетера (балонная ангиопластика). В месте стеноза баллончик раздувается, раздавливая атеросклеротическую бляшку, диаметр сосуда сразу увеличивается. Чаще всего после расширения для сохранения проходимости сосуда в коронарную артерию устанавливают специальную конструкцию – стент. Стент – это по сути эндопротез; представляет собой каркас для сосудистой стенки, который остается в сосуде на постоянной основе и не позволяет образоваться стенозу повторно (рестеноз) (рис. 7). С течением времени стент полностью покроется внутренней оболочкой сосуда, станет его частью. Некоторые стенты выделяют небольшие количества лекарственных веществ (стенты с лекарственным покрытием), которые дополнительно снижают вероятность повторного стеноза.

Рисунок 7. Стентирование коронарной артерии.
Ангиопластика со стентированием при необходимости может применяться не только для коронарных артерий, но и для артерий ног, почек, желудочно-кишечного тракта и других органов. Это вариант лечения как при остром сосудистом событии (инфаркт миокарда, острая ишемия конечности), так и при плановой терапии хронических заболеваний, например, стенокардии.
Ангиопластика должна сопровождаться антитромботической лекарственной терапией – как перед вмешательством, так и после. Антитромботическая терапия предотвращает реакцию крови на металл стента в виде внутрисосудистого тромбоза. Как правило, после установки стента требуется принимать комбинацию из двух антитромботических препаратов в течение длительного времени. Продолжительность и характер антитромботической терапии в каждом конкретном случае могут значительно различаться.
Кровоток может быть восстановлен и другим способом – в обход пораженного (суженного) участка с помощью хирургической операции – аортокоронарного шунтирования (АКШ) (рис. 8), если:
- артерия поражена в труднодоступном месте,
- стенозы есть в нескольких участках коронарного русла,
- поражение тяжелое и баллонной дилатацией артерию не восстановить.
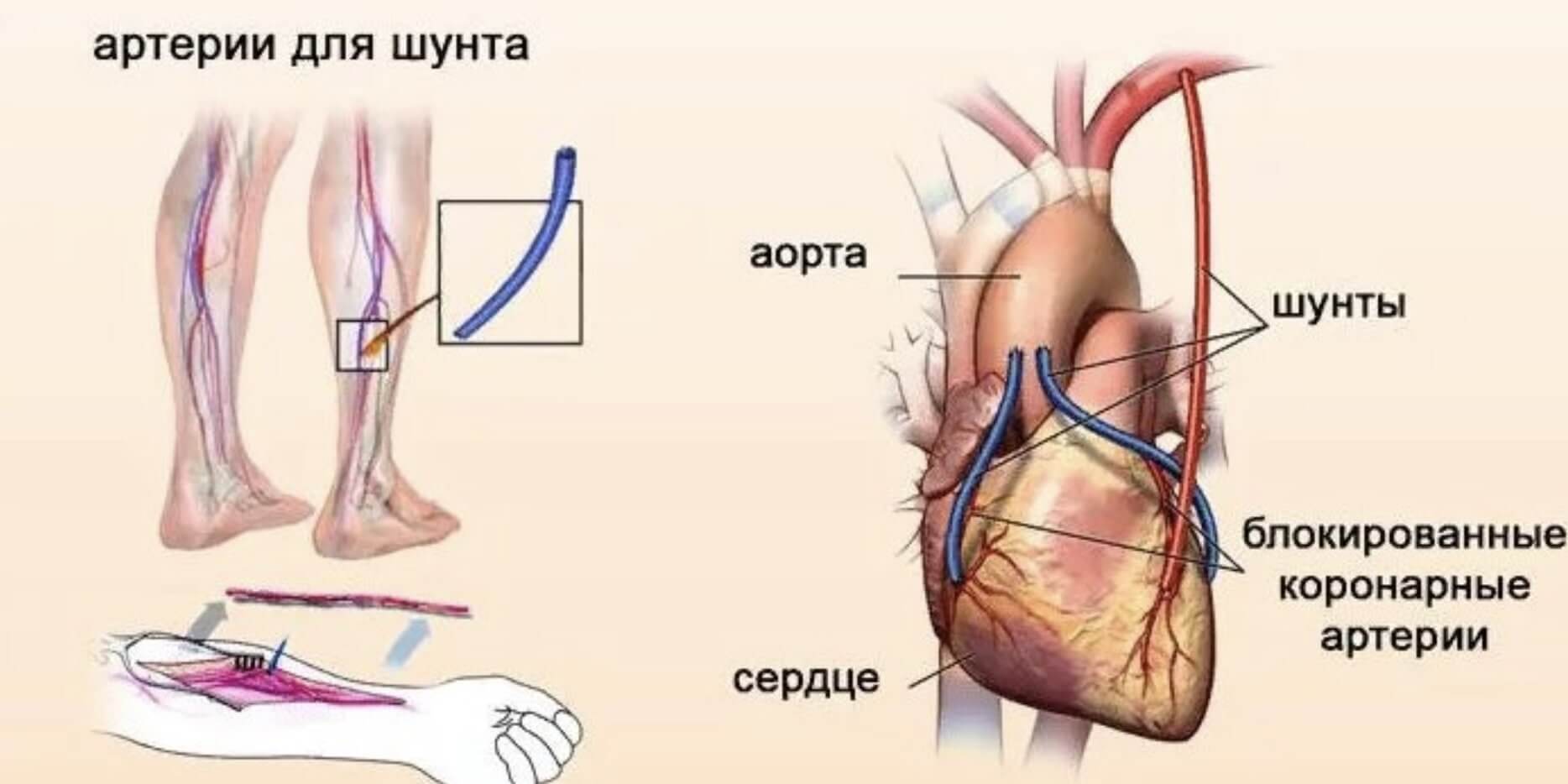
Рисунок 8. Принцип аортокоронарного шунтирования.
Важно своевременно обратиться к врачу – до развития инфаркта миокарда. При ишемической болезни сердца лучшее лечение – предупреждение «сосудистых катастроф». Это позволит сохранить трудоспособность, независимость от посторонней помощи и хорошее качество жизни.
Ишемическая болезнь сердца и ее признак – стенокардия не являются неизбежным сопровождением старения. По исследованиям последних 3-4 десятков лет среди населения несколько снизился риск возникновения стенокардии и инфаркта миокарда. Эта тенденция – заслуга борьбы с известными контролируемыми факторами сердечно-сосудистого риска: высоким артериальным давлением, повышенным уровнем холестерина, сахарным диабетом, табакокурением, малоподвижным образом жизни и ожирением. Особенно заметное снижение заболеваемости произошло в странах, где проводится массовая профилактика атеросклероза и его осложнений, начиная с молодого возраста.
Ишемическая болезнь сердца
Инфаркт миокарда
Инфаркт миокарда – грозное осложнение атеросклеротической болезни сердца – гибель (некроз) клеток сердечной мышцы. Инфаркт начинается, когда сосуд, доставляющий кровь к той или иной области сердца (коронарная артерия), закупоривается тромбом. Чаще всего тромб образуется в области надрыва атеросклеротической бляшки (участок стенки сосуда, где долго откладывался холестерин, – слабое место сосудистой стенки). При этом клетки той части сердечной мышцы, за которую отвечает конкретная артерия, повреждаются из-за сильного кислородного голодания (острая ишемия и повреждение миокарда) (рис. 9).

Рисунок 9. Острый инфаркт миокарда – осложнение атеросклероза.
Если не принять срочные меры, повреждение становится необратимым и клетки погибают, мы констатируем инфаркт миокарда. Таким образом, в данной ситуации несоблюдение режима покоя и отсрочка оказания медицинской помощи опасны для жизни. К счастью, при своевременном и качественном лечении прогноз можно улучшить.
Интенсивная боль в груди, сопровождающаяся страхом смерти, – повод заподозрить острый инфаркт миокарда. Характер боли, результаты электрокардиограммы (ЭКГ), анализ крови на кардиоферменты призваны подтвердить или исключить диагноз. Если инфаркт подтвержден, лечение начинается немедленно и может включать следующие мероприятия:
- попытка восстановления кровотока в артерии с помощью препаратов, растворяющих тромбы, либо механическое расширение артерии с помощью специального баллона (ангиопластика) и по возможности ликвидация тромба при экстренной коронароангиографии,
- профилактика дальнейшего тромбообразования (антитромботические препараты),
- другие лекарства эффективные, как в остром периоде инфаркта, так и в дальнейшем: бета-блокаторы, ингибиторы АПФ, статины (препараты, снижающие уровень холестерина) и др.,
- симптоматическая терапия.
Необходим контроль состояния пациента с помощью мониторирования ЭКГ, чтобы вовремя распознать жизнеугрожающие нарушения ритма сердца, как возможное последствие ишемии (недостаточного кровоснабжения сердца).
В свете сказанного понятно, почему госпитализация больного с острым инфарктом миокарда или серьёзным подозрением на него обязательна.
Больным, перенесшим инфаркт миокарда, для профилактики повторных событий обязательно рекомендуют изменение образа жизни раз и навсегда: отказ от курения, рацион питания с ограничением продуктов, содержащих холестерин, регулярную и адекватную состоянию здоровья физическую активность, лечебную физкультуру.
Однако некоторые пациенты с факторами сердечно-сосудистого риска не следуют рекомендациям по изменению образа жизни. Некоторые убеждены: «Со мной такого не случится». В данном случае отрицание опасности подобно поведению водителей, злостно нарушающих ПДД. При установке «плохие вещи случаются только с другими» внезапное столкновение с суровой реальностью может вызвать психологический шок. Это происходит «вдогонку» инфаркту, который сам по себе часто сопровождается очень сильной болью.
Иногда инфаркт случается при отсутствии факторов риска, либо если факторы риска давно взяты под контроль, что способствует формированию у больного человека ощущения несправедливости, беспомощности в «борьбе с судьбой» и порой приводит к временной утрате доверия к врачам.
После инфаркта нередко развивается депрессия, которая может быть непродолжительной или наоборот стойкой и даже прогрессировать. Это состояние необходимо выявлять и лечить, так как биологические эффекты депрессии могут ухудшить прогноз, в том числе и вследствие высокой вероятности несоблюдения врачебных рекомендаций пациентами с такой проблемой. Существует ряд эффективных методов лечения депрессии (не только фармакологических). Обсуждение темы депрессии с врачом – залог получения своевременной и адекватной помощи.
Застойная сердечная недостаточность
Сердечная недостаточность – состояние, при котором сердце не может перекачивать столько крови, сколько необходимо для работы организма. Причина, как правило, в том, что сердечная мышца не сокращается «как надо».
Сердечную недостаточность могут вызывать различные сердечно-сосудистые заболевания – ишемическая болезнь сердца, патология сердечной мышцы, клапанов сердца, пороки развития магистральных сосудов и др.
При сердечной недостаточности у пациента возникает множество симптомов (рис. 10), ограничивающих повседневную активность, а периодически – острые состояния, требующие госпитализации.

Рисунок 10. Симптомы сердечной недостаточности.
Когда проблема возникает в левом желудочке – возникает левожелудочковая сердечная недостаточность. В этом случае появляются симптомы застоя в легких – одышка (нехватка воздуха) при физической нагрузке и/или кашель также в основном при физической активности. При кашле может выделяться мокрота розового цвета (вследствие примеси крови). Если вовремя не распознать симптомы и не начать лечение, чувство нехватки воздуха усугубится и будет возникать при небольших физических усилиях и даже в покое, особенно в положении лежа. Если поражен правый желудочек (правожелудочковая сердечная недостаточность), происходит накопление жидкости в плевральной полости, появляется ощущение тяжести или боль в правом подреберье (увеличение печени), увеличение живота вследствие за счет накопления жидкости, отеки стоп и голеней. Как при поражении одного, так и обоих желудочков, пациент будет ощущать повышенную утомляемость. В тяжелых случаях может потребоваться госпитализация.
Стратегия лечения, направленная на улучшение переносимости нагрузок, сохранение качества жизни и, по возможности, трудоспособности, включает:
- устранение или уменьшение выраженности симптомов,
- лечение причин сердечной недостаточности,
- физическую и психологическую адаптацию к возникающим ограничениям.
При своевременном начали лечения больше шансов дольше поддерживать хорошее качество жизни.
Арсенал лекарственных препаратов довольно широк. Врач подберет индивидуально эффективную схему поддерживающей медикаментозной терапии сердечной недостаточности. При обязательном последующем наблюдении (визиты к врачу должны иметь определенную периодичность) проводится необходимая коррекция терапии.
Нефармакологические лечебные меры важны и включают диету с ограничением либо полным исключением поваренной соли и лечебную физкультуру с учетом функционального класса сердечной недостаточности. Может потребоваться консультация психотерапевта, специалиста по реабилитации, диетолога, которые будут контролировать привычки пациента, подберут индивидуальную программу физических тренировок, помогут стабилизировать психоэмоциональный фон и адаптироваться к наилучшему из возможных варианту образа жизни. В зависимости от причин ХСН, могут применяться специфические меры, например, лечение нарушений сердечного ритма, а также реконструкция (хирургическая) клапанов сердца и др.
Аортальный стеноз
Аортальный стеноз – сужение просвета аортального клапана. Этот распространенный приобретенный порок обусловлен дегенеративными изменения в клапане обычно из-за накопившихся к пожилому возрасту отложений кальция. При этом аортальный клапан сам по себе становится препятствием выбросу крови из сердца в аорту. В качестве компенсации сокращения сердечной мышцы становятся мощнее, быстрее, но со временем сердечный выброс все же снижается и не может удовлетворить потребности организма, особенно при повышенной физической нагрузке (беге, подъеме по лестнице и т.п.) (рис. 11).
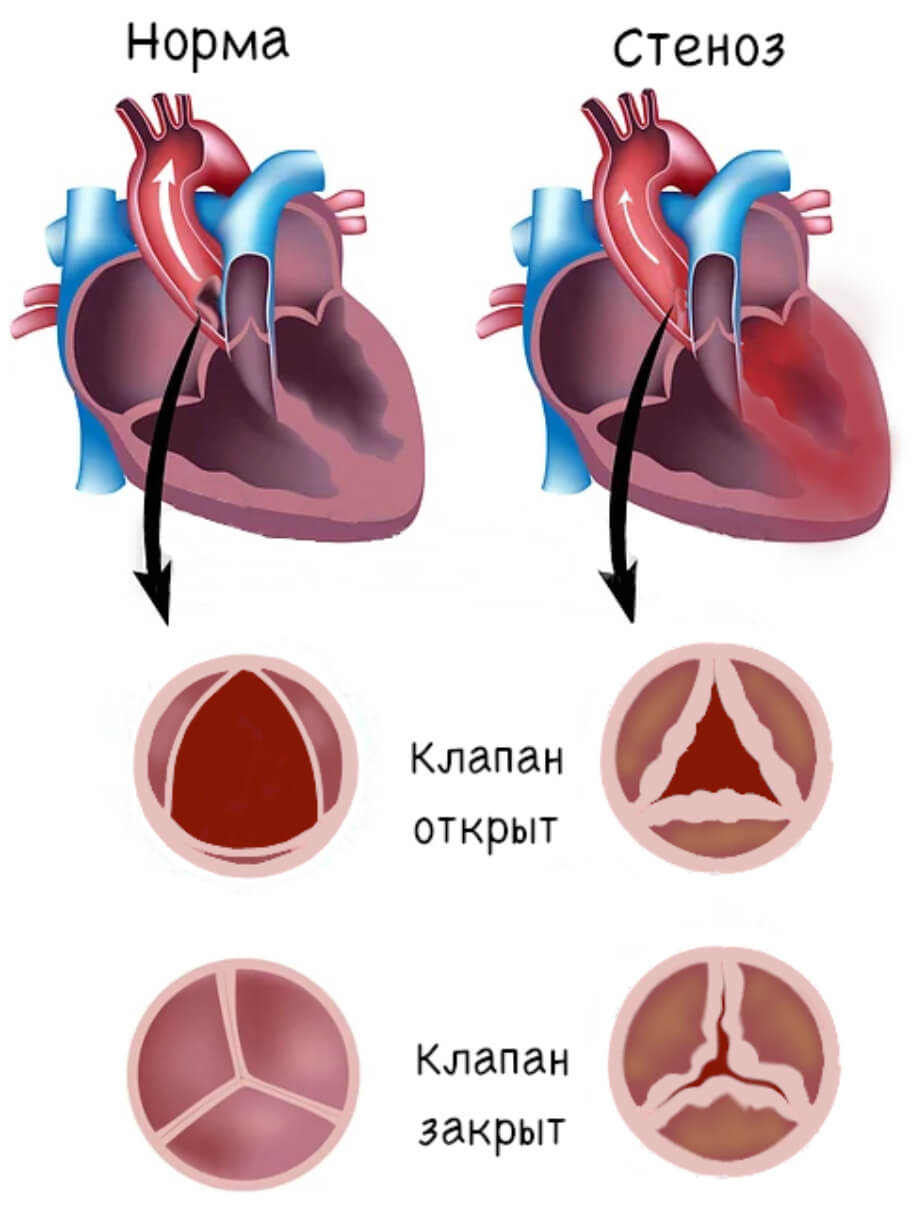
Рисунок 11. А) сердце в норме; Б) сердце при аортальном стенозе.
Обычно стеноз формируется медленно и довольно долго остается бессимптомным; лишь при аускультации (прослушивании) тонов сердца во время осмотра врач может услышать особый шум. Для подтверждения диагноза и оценки степени стеноза используется ультразвуковое исследование сердца (эхокардиография) со специальным допплерографическим анализом (измерение потоков крови и градиентов давления на клапанах сердца). Площадь просвета клапана аорты в норме ≈2,5 см2. Если площадь составляет 1 см2 и менее, сомневаться в диагнозе не приходится.
Возможные симптомы и признаки типичны: появление при физической нагрузке одышки, приступа стенокардии, головокружения, общей слабости и даже иногда потерю сознания.
Болезнь склонна к прогрессированию, спонтанного улучшения ждать не следует. При ухудшении течения, даже если симптомы проявляются только при нагрузке, необходимо лечение.
Возможности медикаментозной коррекции состояния весьма ограничены. Основной подход – хирургическое удаление пораженного клапана и замена его протезом – биологическим или механическим. Механические протезы перед биологическими имеют преимущество – почти неограниченный срок службы. Однако, есть и недостаток – пожизненный прием антикоагулянтов и связанные с этим ограничения и условия. Биологический протез приема антикоагулянтов не требует, но его срок службы – всего 10 лет.
Последние несколько лет введена в практику имплантация биопротеза клапана чрескожным доступом (операция TAVI). Манипуляции в сердце выполняются через введенный в сосуд на руке или ноге катетер – как при коронароангиографии. При успехе операция на открытом сердце не нужна. Пока такие процедуры – альтернатива основному подходу, которой остается «большая» хирургия, хотя показаний для операции TAVI становится все больше в соответствии с результатами успешных клинических испытаний.
Тромбоэмболия легочной артерии (ТЭЛА)
Тромбоэмболия легочной артерии – закупорка тромбом одной из легочных артерий.
Обычно тромб, образуясь в системе периферических вен, перемещается к правой половине сердца, через которую проникает в легочную артерию. Чаще всего тромбы возникают в варикозно расширенных, воспаленных венах ног (при флебитах) обычно за 3-5 дней до развития ТЭЛА (рис. 12).

Рисунок 12. Закупорка легочной артерии тромбом из воспаленной вены нижней конечности.
Следует иметь ввиду, что риск тромбозов и тромбэмболии высок при длительном пребывании в сидячем или лежачем положении (переломы, пребывание ноги в гипсе, длительные поездки на автомобиле или авиаперелеты, малоподвижный образ жизни), при ожирении, беременности, обезвоживании, наличии злокачественных новообразований и не только. Также риск повышается, если вы неправильно принимаете противозачаточные средства, гормональную терапию либо курите. Образование тромбов возможно и при расстройствах системы свертывания крови (тромбофилиях), которые порой носят наследственный характер.
Признаки ТЭЛА – внезапная одышка, боль в грудной клетке, учащенное сердцебиение, возможно кровохарканье. Заболевание может развиваться остро или постепенно, в течение нескольких часов или дней. В тяжёлых случаях развитие ТЭЛА происходит стремительно, сопровождается цианозом (посинением) лица и верхней половины тела, падением артериального давления, может привести к резкому ухудшению состояния и гибели больного. После тяжелого эпизода ТЭЛА может сформироваться правожелудочковая недостаточность кровообращения, проявляющаяся увеличением печени, отёками стоп и голеней, скоплением жидкости в брюшной полости, грудной клетке, сердечной сумке.
Как угрожающее жизни состояние ТЭЛА требует экстренной госпитализации.
Многие годы «золотым стандартом» для подтверждения (либо исключения) ТЭЛА остается КТ-ангиография грудной клетки. При невозможности ее выполнения возможно проведение планарной вентиляционно-перфузионной сцинтиграфии лёгких. Наиболее информативным методом, позволяющим определить, как факт эмболии, так и объём поражения, является зондирование правых отделов сердца и ангиопульмонография.
При острой ТЭЛА могут предприниматься попытки медикаментозного растворения тромбов (системная тромболитическая терапия), при ее невозможности – восстановление проходимости закупоренных артерий путем механического удаления тромбов. Во всех случаях обязательно назначается антикоагулянтная терапия той или иной длительности. При невозможности назначения антикоагулянтов, а также неэффективности обычных доз этих препаратов, проводится имплантация венозных фильтров (кава-фильтров), улавливающих тромбы (рис.13).

Рисунок 13. Принцип установки кава-фильтра для профилактики повторных эпизодов ТЭЛА.
Естественно, для профилактики повторных эпизодов необходимо лечить причину возникновения ТЭЛА.
Больным, перенесшим ТЭЛА, необходимо исключить острую, жирную и высокоуглеводную пищу, а также значительно ограничить продукты с высоким содержанием витамина К, стимулирующего свёртывающую систему (зелень, крапиву, белокачанную и цветную капусту, отруби, злаковые, броколли, оливковое масло, молоко, творог). По рекомендации врача проводятся индивидуально подобранные немедикаментозные профилактические мероприятия.
Фибрилляция предсердий («аритмия»)
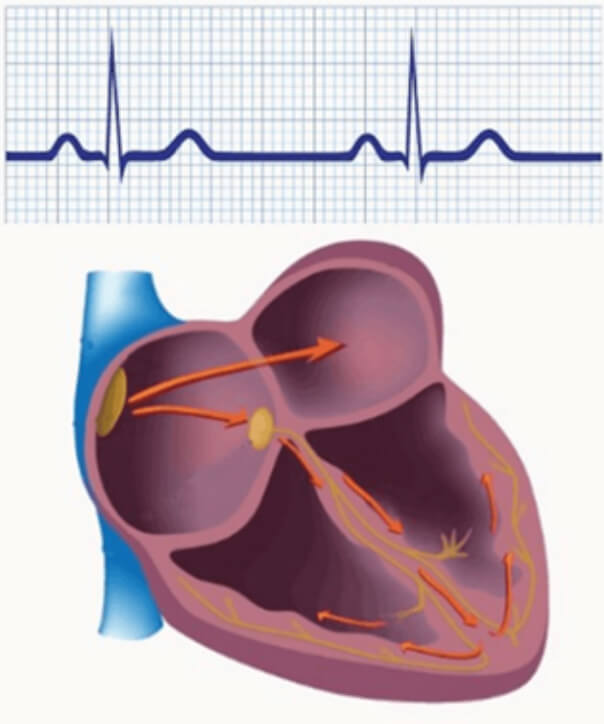
Фибрилляция предсердий (ФП), она же мерцательная аритмия – распространенное наджелудочковое нарушение сердечного ритма и проводимости; представляет собой очень частые хаотичные сокращения различных участков предсердий вследствие нарушения распространения возбуждения по миокарду предсердий с потерей активного выброса крови в желудочки (рис. 14). Выброс крови из желудочков в магистральные артерии сохраняется, но становится менее эффективным. При этом сокращения желудочков, определяющие сердечный ритм и пульс, приобретают, как правило, аритмичный и учащенный характер.
А

Б
Рисунок 14. Нарушение электрической активности предсердий при фибрилляции предсердий.
А – Синусовый ритм (норма); Б – фибрилляция предсердий.
Факторы риска фибрилляции предсердий – это возраст, болезни сердца и сосудов (патология митрального клапана, артериальная гипертензия, сердечная недостаточность), а также многие некардиологические заболевания (острая алкогольная интоксикация, нарушение функции щитовидной железы, тромбоэмболия легочной артерии, непереносимость лекарств, прием наркотических веществ, в частности, кокаина).
Фибрилляция предсердий может иметь непрерывный характер (постоянная форма) или возникать в виде приступов различной продолжительности (пароксизмальная и персистирующая формы). При этом человек может ощущать аритмичное и/или учащенное сердцебиение, возможна боль в грудной клетке, похожая на стенокардию, и признаки сердечной недостаточности (одышка, утомляемость). Возможно и бессимптомное течение, в этом случае нарушение ритма сердца выявляется случайно при медицинском осмотре. Основной метод диагностики – регистрация электрокардиограммы (ЭКГ).
Без нормальных сокращений в предсердиях застаивается кровь, и могут образовываться сгустки крови – тромбы, которые сразу попадают в магистральный кровоток, вызывая тяжелые последствия в виде системной эмболии (закупорка артерий разных сосудистых бассейнов), провоцируя развитие инфарктов внутренних органов и/или головного мозга (кардиоэмболический инсульт) (рис. 15).
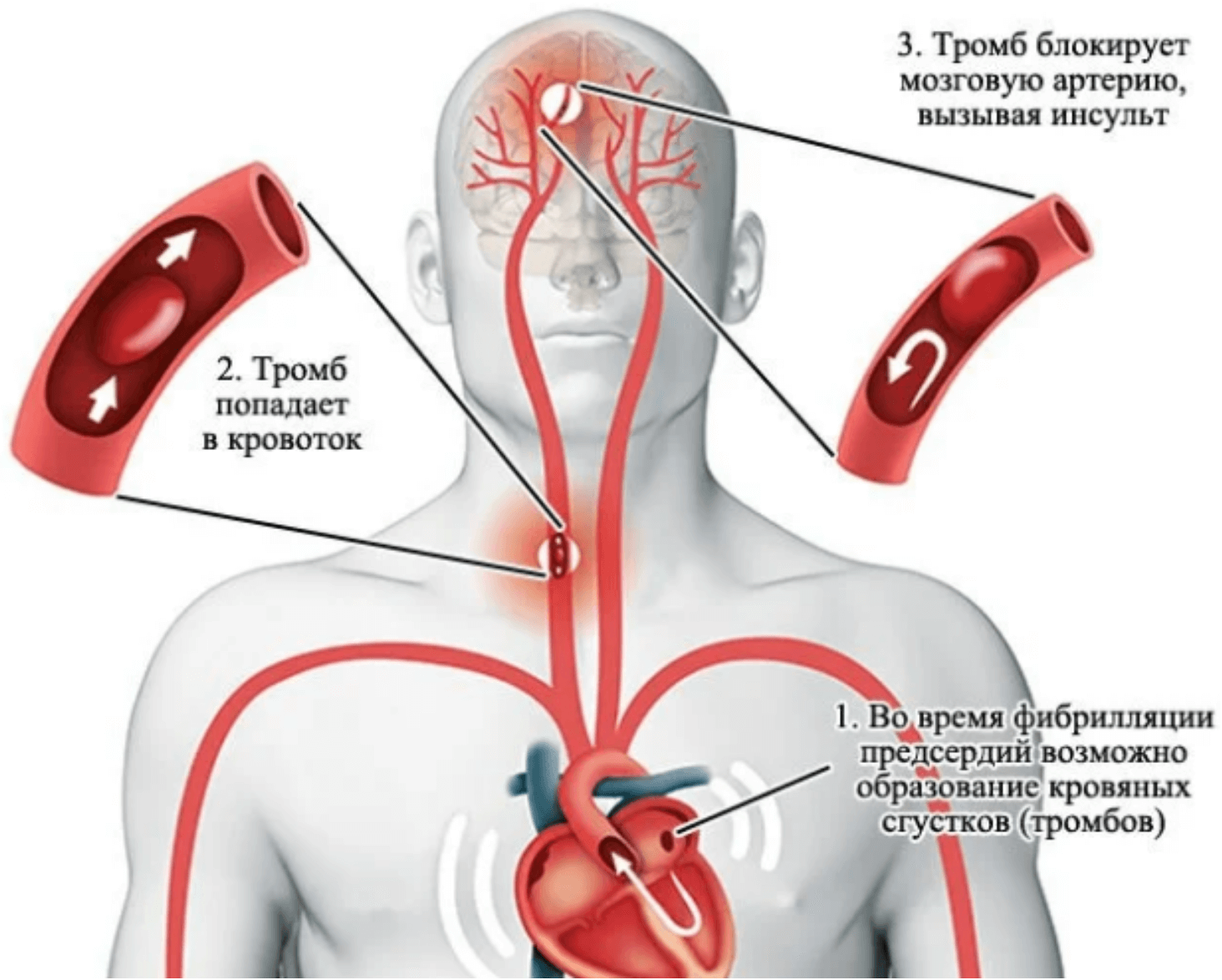
Рисунок 15. Инсульт – частое осложнение фибрилляции предсердий.
Стратегия лечения ФП зависит от ее типа (пароксизмальная, персистирующая, постоянная), давности развития, причины возникновения и состояния сердечно-сосудистой системы.
В одних случаях лечение направлено на купирование приступа аритмии – контроль ритма сердца. Это делается медикаментозно (медикаментозная кардиоверсия), либо путем подачи электрического разряда под общей анестезией (электрическая кардиоверсия). Когда приступ аритмии купирован, ритм сердца приходит в норму – становится синусовым. Дальнейшая антиаритмическая и иная терапия призвана предотвратить рецидив ФП (контроль ритма).
В других случаях саму аритмию «оставляют как есть», и терапевтические усилия направлены на удержание частоты сокращений желудочков близкой к нормальной – контроль ЧСС (частоты сердечных сокращений).
В большинстве случаев при любой стратегии – контроль ритма, либо контроль ЧСС – необходимо принимать антикоагулянты, которые предотвращают образование тромбов в сосудистом русле и системную тромбоэмболию.
Решение о назначении антикоагулянтов принимает лечащий врач на основе оценки риска, как тромбоэмболии, так и кровотечения. В случае назначения антикоагулянтов проводится обучение больного правилам и условиям, которые необходимо соблюдать при приеме этих препаратов.
В последние годы нередко применяется такой метод лечения, как радиочастотная абляция (РЧА) – инвазивная процедура с крайне малым риском осложнений, позволяющая уменьшить вероятность повторных приступов ФП, иногда – до нулевой.
Специальный катетер с функцией генерации тока высокой частоты проводится под контролем рентген-аппарата по артериям внутрь камер сердца, где точечными воздействиями переменным током средней частоты (в диапазоне 350-500 кГц) разрушает патологически функционирующие участки миокарда (рис. 16). В ряде случаев может потребоваться повторное аналогичное вмешательство. Выполнение РЧА, как правило, не исключает необходимости последующей профилактической антиаритмической и антикоагулянтной терапии.
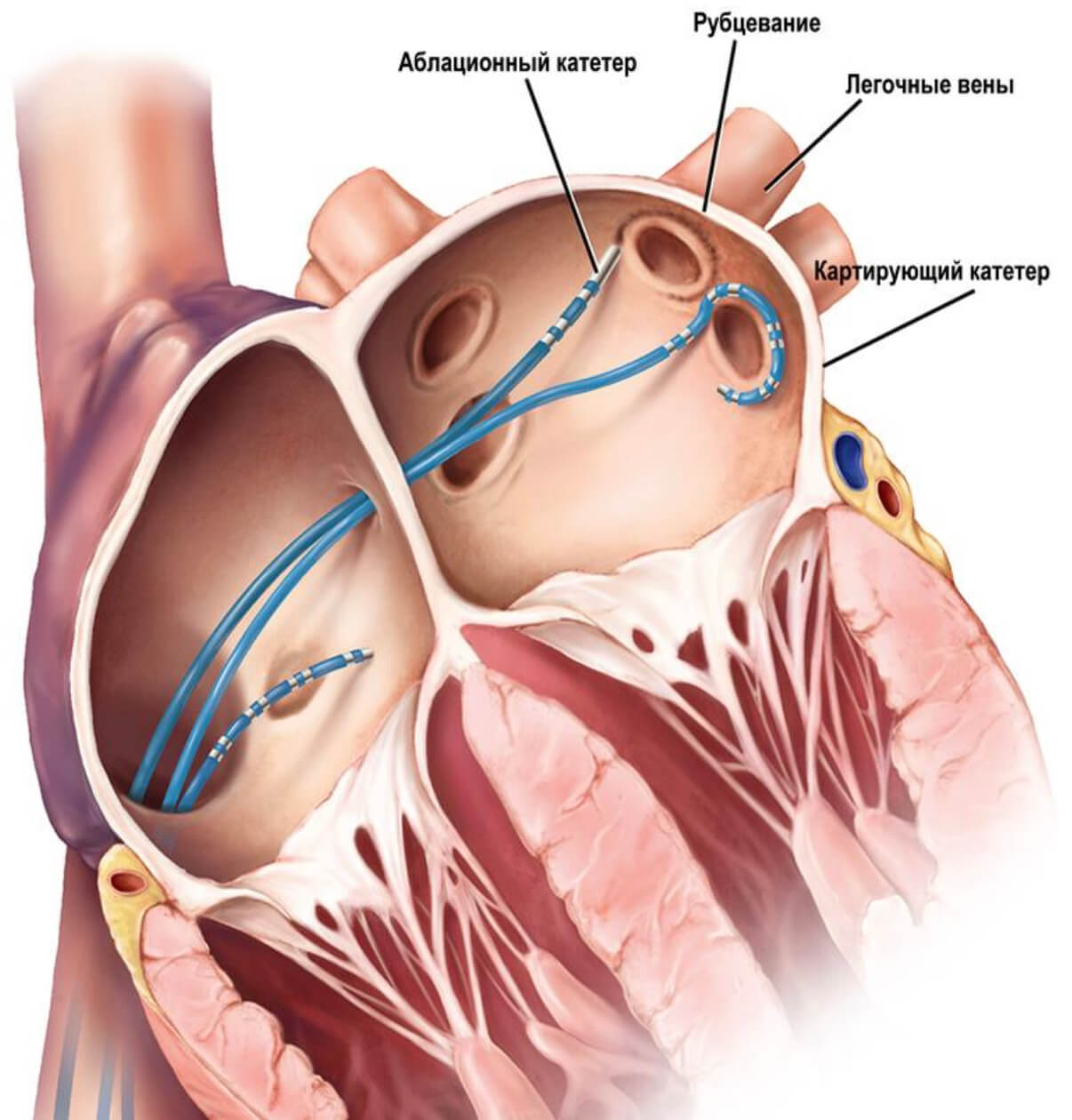
Рисунок 16. Процедура радиочастотной абляции при фибрилляции предсердий.
Кардиостимулятор
Искусственный водитель ритма – электрокардиостимулятор (ЭКС) – устройство, имплантируемое в тело и генерирующее электрические импульсы с доставкой непосредственно в сердце. Необходимость в этом возникает, когда самостоятельных сокращений сердца недостаточно для нормальной жизнедеятельности. Такая операция – метод выбора при различных нарушениях сердечного ритма, например, при полной атриовентрикулярной блокаде.
Первая имплантация кардиостимулятора произведена около 50 лет назад.
Кардиостимулятор – небольшая коробочка в виде корпуса с одним или более электродов. У стимулятора есть собственный элемент питания (обычно – литий-ионный аккумулятор). Электроды берут начало в корпусе кардиостимулятора и другим концом вживляются в стратегически важные участки сердца (верхушка правого желудочка, боковая стенка правого предсердия и др.). Кардиостимулятор устанавливают под местной либо общей анестезией. Корпус устройства располагается под ключицей, а его электроды проходят через вены грудной клетки в камеры правой половины сердца (правое предсердие либо правый желудочек) (рис. 17).
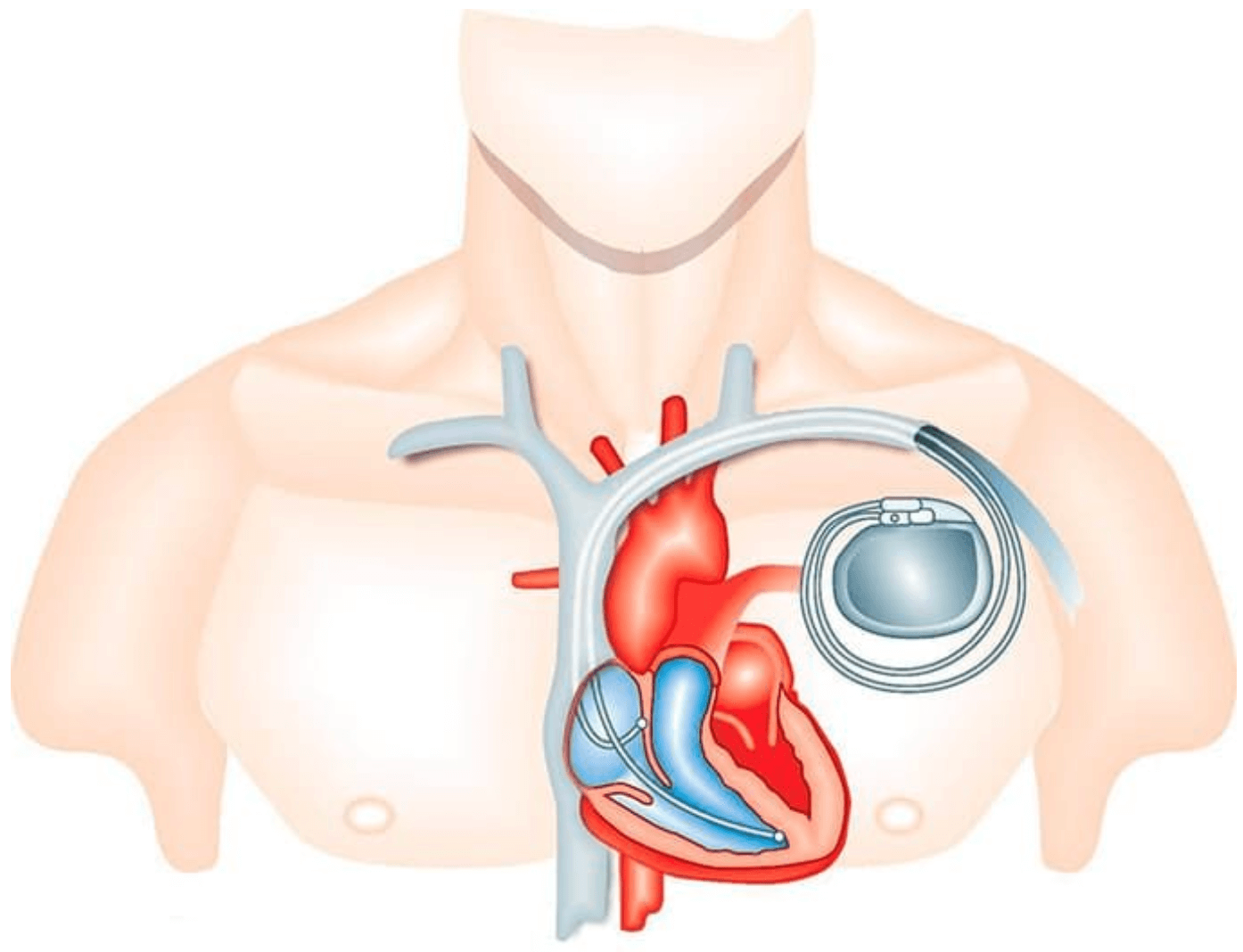
Рисунок 17. Принцип установки кардиостимулятора.
Современные ЭКС имеют очень небольшие размеры; срок их службы составляет несколько лет, иногда – до десяти. Дважды в год кардиостимулятор нуждается в плановой проверке заряда батареи и правильности режима работы. Когда заряд батареи подходит к концу, меняется только корпус устройства: электроды остаются на своих местах и просто подключаются к новому корпусу. Если у Вас установлен кардиостимулятор, избегайте источников электромагнитного излучения, например, слишком сильного приближения к работающим индукционным плитам. Тем более не следует подносить к корпусу устройства сильнодействующие магниты. Не задерживайтесь, проходя охранные рамки на входах и выходах магазинов. Избегайте методов лечения, связанных с электрическими импульсами. Предупреждайте о наличии у Вас ЭКС охрану при прохождении досмотра в аэропортах и вокзалах, и НИКОГДА не занимайтесь дуговой сваркой.
Большая часть кардиостимуляторов несовместима с использованием магнитно-резонансных исследований и электроскальпелей.
Острое нарушение мозгового кровообращения (ОНМК)
Большинство случаев острого нарушения мозгового кровообращения по природе своей ишемические, то есть вызваны снижем поступления обогащенной кислородом крови в головной мозг, что может привести к инфаркту мозга (ишемическому инсульту). Реже происходит кровоизлияния в мозг (геморрагический инсульт) (рис. 18).

Рисунок 18. Варианты острого нарушения мозгового кровообращения.
При недостаточном кровоснабжении мозга появляется разнообразные неврологические симптомы, характер и выраженность которых зависят от пораженной области и объема поражения. В одних случаях в других теряются двигательные функции частей тела (чаще с одной стороны, реже – с обеих), в других нарушается чувствительность, речь, зрение, затруднение в разговоре или понимание речи; может возникнуть головокружение, тошнота, шаткость; возможны падения, потеря сознания и др. В некоторых случаях явные симптомы отсутствуют (рис. 19).

Рисунок 19. «Признаки опасности» при инсульте.
Если симптомы исчезают спонтанно в течение нескольких секунд, минут или часов – речь идет о транзиторной ишемической атаке (ТИА), другое название – микроинсульт. При сохранении симптомов более суток диагностируется острое нарушение мозгового кровообращения – состоявшийся инсульт.
Инсульт – такая же гонка со временем, как и инфаркт. Чем позже произойдет обращение за медицинской помощью, тем больше клеток мозга погибнет и тем ниже вероятность и качество восстановления мозговых функций.
Если инсульт состоялся, в некоторых случаях симптомы могут исчезнуть в течение нескольких дней, недель или месяцев. Однако нередко последствия инсульта прогрессируют, делая больного зависимым от помощи окружающих, и приводят к инвалидности.
Наличие последствий инсульта в виде хронического неврологического дефицита – двигательных либо речевых нарушений разной степени выраженности и стойкости – подразумевает длительную реабилитацию, успех которой в значительной степени зависит от выполнения пациентом полученным рекомендациям.
Заболеваемость ОНМК снижается в тех странах, где на уровне всей популяции проводится борьба с факторами риска как впервые развившегося, так и повторного инсульта: повышением артериального давления, высоким уровнем холестерина, табакокурением, сахарным диабетом и др.
Нарушения липидного обмена и атеросклероз
Холестерин играет важную роль в деятельности эндокринной системы, обмене витамина D, поддержании гормонального статуса и др. При повышении уровня холестеринсодержащих частиц в крови происходит их отложение с выпадением кристаллов холестерина во внутренней оболочке сосудистой стенки (интиме) в виде липидных пятен и полосок. Липидные полоски не вызывают заметной обструкции кровотока и не сопровождаются какими-либо симптомами. Этот процесс носит универсальный характер, поражая различные сегменты артериального русла у людей разного возраста. Так, начальные признаки поражения аорты обнаруживают уже в детстве, липидные полоски – в возрасте 15 лет, а в 30 лет – в сосудах мозга. В дальнейшем липидные полоски увеличиваются в размерах, захватывая все большую поверхность (к 25 годам занимая до половины поверхности аорты)(рис. 1).

Рисунок 1. Этапы развития и последствия атеросклероза.
Со временем под действием классических факторов риска (курения, гиперхолестеринемии, воспалительных процессов, артериальной гипертензии, сахарного диабета, старения, менопаузы и др.) нарушается барьерная и другие функции сосудистой стенки, результатом чего становится трансформация описанных липидных полосок и пятен в атеросклеротические бляшки. Возникает заболевание, именуемое атеросклерозом. В типичных случаях бляшка твердой консистенции имеет очертания купола матового оттенка и выдается в просвет сосуда, суживая его. Бляшка состоит из центральной части – атеромы, образованной из внеклеточного жира, кристаллов холестерина, кальция, остатков погибших клеток, и «покрышки» – фиброзно-мышечного слоя. При фиброзе бляшки атеросклероз становится необратимым, приводит к существенному сужению просвета артерий, длительной ишемии (кислородному голоданию) органов (рис. 2).
Атеросклероз – болезнь скромная и молчаливая, но упорная. Изменения в сосудах могут годами и десятилетиями протекать незаметно для человека. Он может ощущать себя вполне здоровым. Тем временем бляшки растут в артериях, которые питают кровью практически все жизненно важные органы и ткани.
Единые симптомы атеросклероза выделить сложно. Во многом они зависят от того, какие из артерий повреждены больше других. Неизбежными последствиями становятся болевой синдром (в груди, животе, ногах, головная боль), снижение переносимости физических и эмоциональных нагрузок, нарушения ритма сердца, формирование функциональной недостаточности органов, снижение потенции, нарушения памяти и деменция, хромота и даже гангрена нижних конечностей и пр.
Нарушение химического и механического равновесия в бляшке, ослабление ее «покрышки» означают следующую фазу эволюции атеросклероза, характеризующуюся «нестабильностью» повышенным риском разрыва. Бляшка становится более податливой на разрыв по мере увеличения липидного ядра, истончения «покрышки». Разрыв начинается с кровоизлияния в «покрышку» или эрозии стенки артерии. Вероятность разрыва также зависит от расположения, размеров, консистенции и состава липидного ядра бляшки, выраженности местной воспалительной реакции и напряжения стенки сосуда. Триггерами разрыва могут стать рост давления в просвете артерии и/или механическое воздействие кровотока при чрезмерной тахикардии.
Однако и молодые бляшки вследствие наличия в них большого количества полужидких липидов «рыхлы» и нестабильны (прежде всего, их «покрышка») и могут быть гораздо опасней, чем плотная, бедная липидами и склерозированная старая бляшка. Разрыв бляшки с формированием тромба внутри сосуда (атеротромбоз) приводят к развитию сосудистой катастрофы в виде инфарктов органов (сердца, мозга и др.), а также кровоизлияний (рис. 1,2).

Рисунок 1. Атеротромбоз.
Временные клинические последствия атеросклероза мало предсказуемы. Так, долго (десятки лет) имеющаяся бляшка может быть «немой», но затем внезапно развивается острый коронарный инцидент. Бляшки могут расти вдоль сосуда, тогда они развиваются медленно, длительно и менее опасны. Иногда единичные и небольших размеров атеросклеротические бляшки («летальные») располагаются поперек сосуда, приводя к быстрой коронарной катастрофе.
Лечение атеросклероза у взрослых. Чем раньше выявлен атеросклероз и начато лечение, тем лучше будет прогноз. Но важно понимать – лечиться нужно будет всю оставшуюся жизнь, внося серьезные изменения в свой привычный образ жизни. Только так можно существенно затормозить изменения в сосудах и не допустить осложнений.
Ликвидировать фиброз бляшки с помощью лекарственных средств невозможно, но некоторая атеросклеротической бляшке на любой стадии ее развития за счет снижения содержания липидных компонентов. В ряде случаев даже некоторое уменьшение размера бляшки может существенно улучшить течение ишемической болезни и ее исход.
Причин нарушения липидного обмена немало: ряд заболеваний, образ жизни, генетические особенности и некоторые другие. Столкнуться с этой проблемой может человек любого возраста, пола и этнической принадлежности. Повышенный холестериан – опасность, о которой пациент может не знать и не обращаться за помощью, допуская прогрессирование поражения сосудов, кислородное голодание органов и, соответственно, развитие ишемической болезни, чреватой серьезными, инвалидизирующими осложнениями.
О выраженности нарушений обмена липидов и сопутствующих рисках для сердечно-сосудистой системы врач судит по ряду показателей биохимического анализа крови, например, по уровню общего холестерина, холестерина липопротеидов низкой плотности, холестерина липопротеидов высокой плотности, триглицеридов и др. На эти показатели врач ориентируется при выборе мер профилактики атеросклероза и его осложнений, а также при оценке их эффективности. При необходимости будет рекомендовано дополнительное обследование – ряд инструментальных и лабораторных исследований, позволяющих уточнить характер и выраженность уже имеющегося поражения и, соответственно, прогноз для жизни и здоровья.
Известно, что снижение концентрации общего холестерина в крови: снижение концентрации общего холестерина в крови на 10% приводит к уменьшению смертности от заболеваний сердца на 20%.
Профилактика и лечение атеросклероза проводятся комплексно. Главной профилактической мерой является здоровый образ жизни. Различные меры по изменению образа жизни вносят разный по удельному весу вклад в нормализацию липидного обмена и увеличение продолжительности жизни (табл. 1).

Таблица 1. Влияние изменения образа жизни на уровень липидов
Необходимо уделять время ежедневной физической активности: умеренные аэробные нагрузки способствуют нормализации липидного баланса в организме. По поводу вида упражнений, длительности и частоты занятий необходимо посоветоваться с врачом.
Отказ от вредных привычек (курения, употребления алкоголя) позитивно скажется на состоянии сосудов.
Рекомендуется разнообразное питание, способное удовлетворить все потребности организма в витаминах, минералах и других важных веществах. Для снижения уровня холестерина в крови и нормализации липидного баланса, как правило, требуется изменить характер питания. Эффективно уменьшение в рационе доли животных жиров, простых легкоусваиваемых углеводов (мучное, рафинированные сладости) в том числе фастфуда, акцент в питании на рыбу (предпочтение отдают рыбе холодных морей), растительные масла и другие продукты с высоким содержанием омега-3 полиненасыщенных жирных кислот (табл. 2). За составлением рациона лучше всего обратиться к врачу.

Таблица 2. Рекомендации по питанию для улучшения общего профиля липопротеидов
Так как инфекционные и эндокринологические заболевания повышают риск развития атеросклероза, важно ежегодно проходить общий медицинский осмотр для своевременной диагностики и лечения. Условно здоровым людям после 40 также рекомендуется 1) раз в год сдавать анализ крови на холестерин: это позволит выявить нарушения на ранних этапах; 2) проверить уровень в крови такого липидного показателя как липопротеид (а), в значительной мере детерминированный генетическими причинами.
Медикаментозная коррекция дислипидемии. Статины – это группа препаратов, действие которых основано на блокировании образования холестерина в печени, что снижает его уровень в крови, так как весь холестерин, используемый организмом, вырабатывается именно там, а не поступает с пищей. Тот холестерин, что мы получаем с продуктами животного происхождения является только материалом для синтеза собственного. Длительное (пожизненное) лечение статинами при условии оптимальной интенсивности позволяет снизить уровень атерогенного холестерина на 30-50%. Фибраты – другая группа препаратов, снижающих выработку липидов, особенно триглицеридов, в организме. Используются также средства, которые уменьшают всасывание жира из пищевых продуктов в кишечнике, что позволяет добиться дополнительного снижения уровня атерогенных липидных частиц на 10-15%.
Помимо перечисленного по показаниям проводится медикаментозная профилактика тромбозов; при необходимости применяются препараты для устранения симптомов.
В случаях тяжелого поражения может быть рекомендовано хирургическое лечение – баллонная ангиопластика (сосуд растягивают специальным баллончиком), стентирование (в просвет суженного сосуда ставят сеточку-каркас, который расширяет просвет) и др.
В определенных случаях базовые меры по поддержанию здорового образа жизни и стандартная медикаментозная терапия не помогают поддерживать холестерин крови на должном уровне. Причина может заключаться в генетическом характере нарушений липидного обмена. В этом случае диагностический подход может включать углубленное обследование, в том числе молекулярно-генетический анализ, консультирование членов семьи с целью выбора стратегии и тактики лечения, которое поможет увеличить продолжительность жизни и улучшить ее качество.
